Результаты работы исследовательской группы Центра Джона Иннеса дополняют понимание устойчивости к противомикробным препаратам, одной из главных угроз для глобального общественного здравоохранения.
Ученые из группы профессора Тони Максвелла изучили более ранние исследования, которые показали, что воздействие низких доз хинолоновых антибиотиков может привести к развитию у бактерий устойчивости к другим, неродственным антибиотикам.
Хинолоны - широко используемые антибиотики, которые воздействуют на фермент ДНК-гиразу, необходимый для выживания бактерий. Понимание механизмов устойчивости, вырабатываемых патогенами к антибиотикам, является жизненно важным направлением стратегии, необходимой для разработки эффективных новых лекарств.
Благодаря широкому антибактериальному спектру, высокой эффективности, низкой токсичности и хорошей пероральной абсорбции хинолоны, класс синтетических антибактериальных средств с базовой структурой 1,4-дигидро-4-оксохинолин-3-карбоновой кислоты, широко используются в аквакультуре, животноводстве и лечении заболеваний человека.
Команда хотела выяснить, соответствует ли действительности описанное явление антибиотикорезистентности, вызванной хинолонами (QIAR), и если да, то какие из существующих типов хинолонов могут быть в этом замешаны. Исследователи также хотели понять молекулярные механизмы, которые позволяют бактериям вырабатывать устойчивость к этим жизненно важным препаратам.
В экспериментах использовались бактерии E. coli, подвергнутые воздействию нелетальных концентраций четырех видов хинолонов (ципрофлоксацина, моксифлоксацина, оксолиновой кислоты и норфлоксацина). Затем колонии бактерий подвергались воздействию нехинолоновых антибиотиков и контролировались показатели выживаемости.
Результаты показали, что все протестированные хинолоны могут проявлять QIAR, за исключением моксифлоксацина.
Полное секвенирование генома бактерий показало, что устойчивость может быть обусловлена рядом мутаций в ДНК бактерий, вызванных лечением хинолонами. Результаты показывают, что моксифлоксацин может убивать E. coli с помощью иного механизма, чем другие хинолоны.
В целом работа ученых демонстрирует физиологические механизмы, которые приводят к множественной лекарственной устойчивости у бактерий, что имеет значение для использования антибиотиков в медицине и сельском хозяйстве.
Профессор Тони Максвелл, автор исследования, сказал: «Наши результаты показывают, что особенно важно избегать воздействия низких доз хинолонов - доз ниже тех, которые обычно убивают бактерии. Это может произойти, когда хинолоны неправильно или чрезмерно используются в медицине или в немедицинских целях, например, в сельском хозяйстве или фармацевтической промышленности, загрязняя окружающую среду».
Устойчивость к противомикробным препаратам возникает, когда такие лекарства, как антибиотики, противовирусные и противогрибные препараты, больше не эффективны против патогенов. Это естественный процесс, который происходит из-за естественных изменений патогенов, но он ускорился из-за чрезмерного и неправильного использования противомикробных препаратов.
По оценкам, если не принять меры по устранению этой угрозы, к 2050 году устойчивость к противомикробным препаратам станет причиной 10 миллионов смертей в год и обойдется мировой экономике в 10 триллионов долларов США в плане экономического производства.
Всемирная организация здравоохранения определила рациональное использование антибиотиков, а также научные исследования и разработки в области антибиотиков как ключевые направления борьбы с устойчивостью к противомикробным препаратам.
Источник: John Innes Centre.
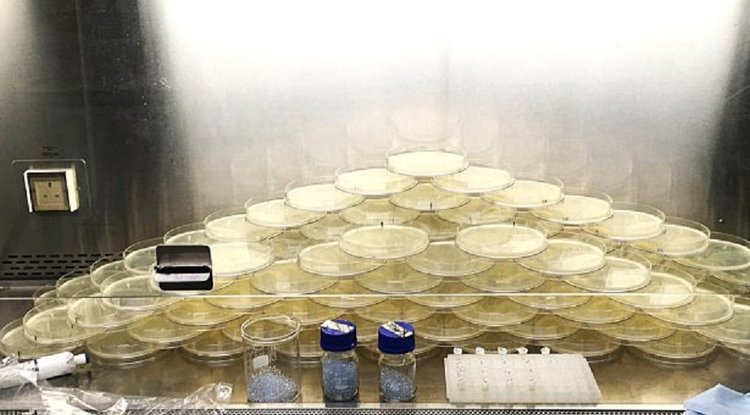
На фото - чашки с агаром, использованные в одном эксперименте, где бактерии E. coli подвергались воздействию низких доз хинолоновых антибиотиков перед отбором на устойчивость к нехинолоновым антибиотикам. Автор фото: Наташа Буш.