Химические классы пестицидов
Оглавление
- Физические и химические свойства
- Действие на вредные организмы
- Механизм действия
- Симптомы повреждения
- Подавляемые сорные виды
- Резистентность
- Профилактика резистентности
- Применение
- Токсикологические свойства и характеристики
Физические и химические свойства
Фениловые эфиры – органические соединения, образованные при участии фенолов (С6Н5ОН). При этом в образовании как простых (общая формула R–O–R’), так и сложных эфиров, (RCO2R'), фенол участвует только водородом гидроксильной группы (-ОН)[5].
Наиболее простой способ получения фениловых эфиров – через феноляты (солеобразные соединения, получаемые замещением водорода гидроксильной группы фенолов металлами, например, фенолят натрия – C6H5ONa)[5]. В результате реакции получают органическую соль и искомый фениловый эфир. Так при взаимодействии хлорангидрида уксусной кислоты C2H3ClO и фенолята натрия C6H5ONa получают хлорид натрия NaCl и фениловый эфир уксусной кислоты C6H5O-С=ОCH3)[5].
Фениловые эфиры обычно рассматривают как органическое соединение, образованное фенокси группой с любыми другими сочетаниями органических радикалов при присоединениии этих радикалов по атому кислорода[5].
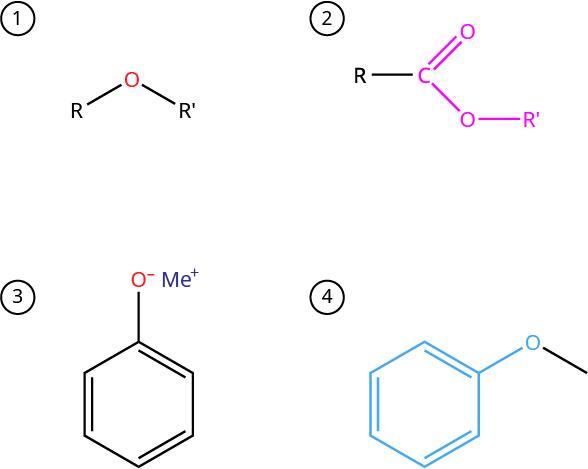
1. Общая формула простых эфиров
2. Общая формула сложных эфиров
3. Общая формула фенолятов (Ме – металл)
4. Фенокси группа[6]
Фениловые эфиры можно рассматривать как фенолы, со всеми присущими им химическими и физическими свойствами. Кроме того, многие сложные соединения, включающие с структурную формулу фенил-радикал в сочетании с «эфирной группой» -О- или O=C-O, может рассматриваться как фениловый эфир. Однако индивидуальные химические и физические свойства такого вещества будут во многом зависеть от других органических и неорганических радикалов, входящих в их структурные формулы[5].
По классификации HRAC (Herbicide Resistance Action Comittee/Комитет по борьбе с устойчивостью к гербицидам) и WSSA (Weed Science Society of America/Американское научное общество по борьбе с сорняками) в пределах класса фениловые эфиры рассматриваются действующие вещества гербицидов: дифлюфеникан, бефлубутами, пиколинафен[7].
Дифлюфеникан C19H11F5N2O2 (номер CAS 83164-33-4) из-за сложности структурной формулы в различных источниках рассматривают как пиридины, пиридинкарбоксамиды, пиридонкарбоксамиды, никотиннанилиды, карбоксамиды, амиды[4][6][8]. В классификации HRAC и WSSA после 2020 дифлюфеникан отнесен к классу фениловые эфиры[7].
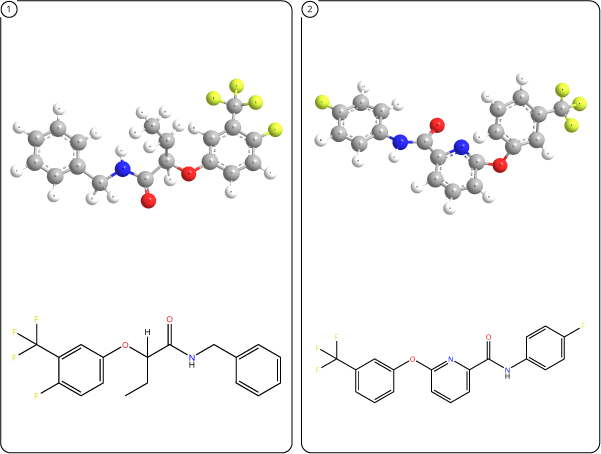
Бефлубутамид C18H17F4NO2 (номер CAS113614-08-7) или N-бензил-2-[4-фтор-3-(трифторметил)фенокси]бутанамид рассматривается как амид монокарбоновой кислоты, образующийся в результате формальной конденсации карбоксигруппы 2-[4-фтор-3-(трифторметил)фенокси]масляной кислоты с амино группой бензиламина. Это амид монокарбоновой кислоты, ароматический эфир, является монофторбензолом и трифторметил бензолом. Функционально связан с бензиламином[6].
Пиколинафен C19H12F4N2O2 (номер CAS137641-05-5) или N-(4-фторфенил)-6-[3-(трифторметил)фенокси]пиридин-2-карбоксамид рассматривается как пиридинкарбоксамид, образующийся в результате формальной конденсации карбоксигруппы 6-(м-трифторметилфенокси)пиколиновой кислоты с амино группой p-фторанилина. Является трифтолметилбензолом, ароматическим эфиром и монофторбензолом[6].
Действие на вредные организмы
Фениловые эфиры могут быть биологически активными веществами. К данному химическому классу классификация HRAC и WSSA относит вещества с гербицидной активностью: дифлюфеникан C19H11F5N2O2 (номер CAS83164-33-4) и бефлубутамид C18H17F4NO2 (номер CAS113614-08-7), пиколинафен C19H12F4N2O2 (номер CAS137641-05-5)[7][6].
Механизм действия
. По классификации HRAC (Herbicide Resistance Action Comittee/Комитет по борьбе с устойчивостью к гербицидам) и WSSA (Weed Science Society of America/Американское научное общество по борьбе с сорняками) все три вышеуказанных вещества относятся к ингибиторам фитоиндезатуразы /inhibition of phytoene desaturase и включены в группу 12, до 2020 года – группа F1[7].Группа 12 включает следующие классы химических веществ: дифенилгетероциклы (Diphenyl heterocycles), N-фенилгетероциклы (N-Phenyl heterocycles), фениловые эфиры (Phenyl ethers)[7].
Фитоиндезатураза – фермен участвующий в синтезе каротиноидов. Поэтому в отечественной литературе дифлюфеникан по механизму действия относят к группе ингибиторы биосинтеза каротиноидов[2]. Дифлюфеникан, бефлубутамид, пиколинафен, подавляя фитоиндезатуразу блокируют синтез каротиноидов[7].
Каротиноиды – жирорастворимые пигменты красного желтого и оранжевого цветов. Они являются обязательными компонентами пигментных систем, для их синтеза не требуется энергия солнечного света. Каротиноиды выполняют функцию защиты фотоситетической пигментной системы от фотоокисления, участвуют в фиксации углекислого газа и расширяют интервал длин волн, вовлекаемых в фотосинтез. Они тесно связаны с белками и липидами мембран[2].
Нарушение биосинтеза каротиноидов приводит к дестабилизации жизнедеятельности растения. В частности, при отсутствии каротиноидов, синглетный кислород (метастабильное состояние молекулярного кислорода), ранее ими связываемый, вступает в реакцию с ненасыщенными липидами (мембранными жирными кислотами, хлорофиллом) и образуют липидный радикал, взаимодействующий с кислородом и образующий периоксид липида и еще один липидный радикал. То есть инициируется самоподдерживающаяся цепная реакция перекисного окисления липидов, которая функционально разрушает хлорофилл и мембрану. Разрушение составных компонентов мембраны приводит к нарушению целостности мембран и быстрому высыханию тканей[7].
Классы химических соединений, по механизму гербицидного действия – ингибиторы фитоиндезатуразы (группа 12 (F1) по классификации WSSA и HRAC):
- Дифенилгетероциклы (diphenyl heterocycles);
- N-фенилгетероциклы (N-phenyl heterocycles);
- Фениловые эфиры (phenyl ethers)[7].
Симптомы повреждения
. Некроз и хлороз листовых пластинок[2].Подавляемые сорные виды
. Однолетние двудольные и злаковые сорные растения[3]. Спект подавляемых видов зависит от свойств конкретного вещества. Подробнее о видах чувствительных к дифлюфеникан – в статье «Дифлюфеникан».Резистентность
. Как ингибиторы синтеза каротиноидов, фениловые эфиры относят к группе среднего риска по формированию резистентных биотопов сорных растений[3]. Формирование резистентных биотопов зафиксировано у видов: редька дикая, арктотека ноготковая[7].Профилактика резистентности
:- соблюдение регламета применения препаратов, содержащих соединения класса фениловые эфиры;
- выбор для чередования препаратов с отличным механизмом действия[3].
По классификации HRAC и WSSA тем же механизмом действия обладают соединения химических классов: дифенилгетероциклы (diphenyl heterocycles), N-фенилгетероциклы (N-phenyl heterocycles), фениловые эфиры (phenyl ethers)[7].
Применение
Соединения, отнесенные по HRAC и WSSA к классу фениловых эфиров, а именно дифлюфеникан, бефлубутамид, пиколинафен, в сфере защиты растений применяют в качестве действующих веществ пестицидов (гербицидов) [7]. Дифлюфеникан разрешен к применению на территории России[1]. Бефлубутамид, пиколинафен – в других странах мира[7].
Токсикологические свойства и характеристики
Соединения, отнесенные по HRAC и WSSA к классу фениловых эфиров, а именно дифлюфеникан, бефлубутамид, пиколинафен характеризуются третьим классом опасности (умеренно опасные) для человека и третьим классом опасности (малоопасные для пчел)[1][8].
Бенфлубутамид:
- ЛД50 орально для крыс > 5000 мг/кг, ЛД50 дерм.> 2000мг/кг. Не раздражат кожу и слизистую глаз кроликов;
- СК50 (14 дн.) для дождевых червей 732 мг/кг. Не токсичен для почвенной микрофлоры;
- период распада в почве (дни): ДТ50 (типичный) – 5,4[8].
Пиколинафен:
- ЛД50(мг/кг) орально для крыс> 5000;
- почвенные черви – острая 14-дневная СК50 (мг/кг)> 1000;
- птицы – острая ЛД50 (мг/кг)> 2250;
- период распада в почве (дни): ДТ50 (типичный) – 30; ДТ50 (лабораторный при 20ºC) – 7,5; ДТ50 (полевой) – 30[8].
Токсикоэкологическая характеристика д.в. дифлюфеникан – в статье «Дифлюфеникан».
2. Дорожкина Л.А. Применение гербицидов и регуляторов роста в защите растений: учебное пособие / Л.А. Дорожкина, Л.М. Поддымкина. – М.: МЭСХ, 2021. – 206 с.
3. Куликова Н.А, Лебедева Г.Ф. Гербициды и экологические аспекты их применения. Учебное пособие. – Москва, книжный дом «ЛИБРОКОМ», 2010. – 152с.
4. Методические указания по регистрационным испытаниям гербицидов, в сельском хозяйстве 2013 г. СПб (утверждены Минсельхозом России). УПДК 632.96, СПб. 2013. 280 с.
5. Харлампович Г.Д., Чуркин Ю.В. Фенолы. М.: Химия, 1974. - 376 с.
6. Pubchem.ncbi.nlm.nih.gov
8. http://www.rupest.ru/