Химические классы пестицидов
Оглавление
Физические и химические свойства
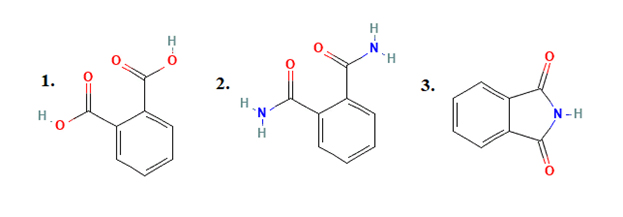
Бензолкарбоксамиды функционально связаны с фталевой кислотой (о-фталевой или 1,2-бензолдикарбоновой кислотой), которая является простейшим представителем двухосновных ароматических карбоновых кислот. («Фталивая кислота. Фталамид. Фталимид». , соединение 1)[1].
Первое соединение гомологического ряда бензолкарбоксамиды – фталамид (диамид фталивой кислоты). («Фталивая кислота. Фталамид. Фталимид». , соединение 2).
Фталамид (диамид фталевой кислоты, бензолдикарбоксамид), в чистом виде, бесцветные кристаллы или грязновато-белый порошок со следующими физическими характеристиками:
- плотность вещества – 1,294 г/см3;
- температура кипения – 430,8ºC;
- температура плавления – 223 ºC;
- температура вспышки – 214,4ºC[8].
Фталамид при пиролизе превращается во фталимид («Фталивая кислота. Фталамид. Фталимид», соединение 3)[7].
Фталамид легко реагирует с различными веществами, в частности с бромом, бензимидазолом, изотиоцианатом, ацетилом, бензотиазолом, изотиоцианатом, диазепином, с образованием соответствующих производных. Присоединение идет в основном по азоту аминогрупп с замещением атомов водорода[7].
Бензолдикарбоксамиды структурно связаны с антраниламидами и могут рассматриваться как диамиды, поскольку в структурной формуле присутствует две амидные группы[10].
Химические классы и соединения, по механизму инсектицидного действия модуляторы рианодиновых рецепторов (группа 28 по классификации IRAC):
Класс – диамиды (diamides).
Действующие вещества:
- Хлорантранилипрол
- Циантранилипрол
- Цикланилипрол
- Флубендиамид
- Тетранилипрол[9]
Действие на организмы
Бензолдикарбоксамиды – достаточно новый класс гетероциклических соединений, исследование биологической активности таких соединений активно ведется во всем мире. Установлено, что различные производные фталамида проявляют антибактериальную активность в отношении грамположительных и грамотрицательных штаммов бактерий кишечной палочки и золотистого стафилокока[7].
На сегодняшний день в сфере защиты растений используется только одно соединение класса бензолдикарбоксамиды – флубендиамид. Он относится к группе диамидов фталевой кислоты[3].
Механизм действия
. По классификации IRAC (Insecticide Resistance Action Committee) флубендиамид относятся к группе 28 (класс диамиды) – модуляторы рианодиновых рецепторов[9].Бензолдикарбоксамиды близки по строению природным веществам: алкалоиду, рианодину и антраниламиду. Они, как и другие диамиды, служат модуляторами рианодинового рецептора, отвечающего за регуляцию нервной и мышечной активности насекомых, связанных с изменением содержания кальция в клетках[3].
Подробнее о механизме действия соединений группы 28 – в статье «Антраниламиды».
При введении в формулу производных фталамида гидразонов (общая формула R1R2C=N−NH2), присутствующих во многих пестицидных соединениях, были получены соединения более эффективные, чем флуобендиамид. Установлено, что они эффективны в качестве кишечных пестицидов против тли (Myzus persicae). Только некоторые из полученных соединений обладали ларвицидной активностью против бриллиантовой моли (Plutella xylostella, Linnaeus)[6].
Симптомы поражения
. При поедании отравленной пищи у насекомых перестают сокращаться мышцы, затем следует паралич, и гибель через 2–4 дня[3].Поражаемые виды
. Различные виды отряда чешуекрылых.[3].Резистентность
. Насекомые, резистентные к фосфорограническим соединениям, карбаматам, пиретроидам, остаются чувствительными к бензолдикарбоксамидам[3].Однако во многих регионах США, Великобритании, Бразилии, Китая, Пакистана,Таиваня, Индии установлены факты формирования резистентности у чешуекрылых к диамидам, и в частности к флубендиамиду[3].
Главными причинами формирования резистентности стали:
- отсутствие ротации инсектицидов;
- отсутствие грамотного севооборота;
- недостаточная дозировка инсектицида;
- ирригация;
- отсутствие стратегий управления устойчивостью к инсектицидам[3].
Подробнее – в статье «Флубендиамид».
Профилактика резистентности
– в статье «Антраниламиды».Фитотоксичность
бензолдикарбоксамиды при соблюдении регламента применения не проявляют[3].Применение
Бензолдикарбоксамиды в последнее время вводят в фармакологию, как бактерийные средства. В сфере защиты растений их применение в настоящее время ограничено соединениями с инсектицидной активностью, но вполне вероятно обнаружение веществ с другими типами биологической активности[7][6].
В настоящее время на территории России разрешены к применению инсектициды с действующим веществом флубендиамид[2].
Получение
Синтез первого в ряду бензолдикарбоксамидов соединения – фталамида, осуществляется следующим способом, состоящим из трех стадий:
- Получение фталиевого ангидрида окислением о-ксилола на катализаторе V2O5– TiO2[4].
- Получение фталимида аммонолизом фталевого ангидрида[4].
- Получение фталамида взаимодействием фталимида и аммиака[4].
Кроме данного разработано ещё несколько способов получения фталамида:
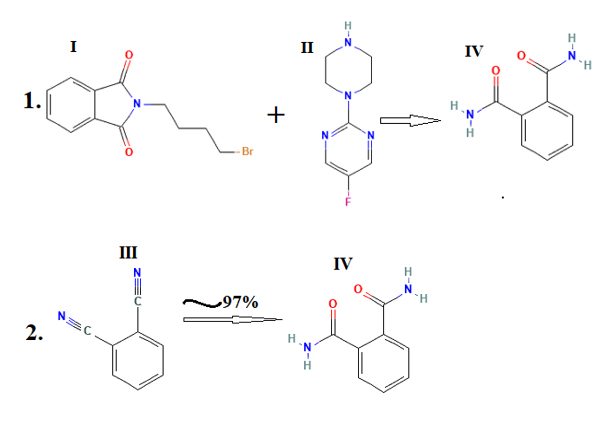
- Взаимодействие N-(4-бромбутил) фталимид с 5-фтор-2-пиперазин-1-илпиримидин (фото Синтез фталамида, реакция 1)[8].
- Путем катализируемой гидратации нитрилов (фталонитрила) в чистой воде при мягких атмосферных условиях. (фото Синтез фталамида, реакция 2)[8].
Бензолдикарбоксамиды получают путем обработки фталамида различными веществами функциональные группы которых желают ввести в его формулу[7][6].
Токсикологические свойства и характеристики
Бензолдикарбоксамиды, используемые в сфере защиты растений характеризуются низкой экологической опасностью. В частности, флуобендиамид относят к умеренно опасным веществам по отношению к человеку и умереноопасным – по отношению к пчелам[2].
Класс опасности:
- 3 – для человека;
- 2 – для пчел[2].
Подробнее – в статье «Флубендиамид».
2. Государственный каталог пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации, 2023 год. Министерство сельского хозяйства Российской Федерации (Минсельхоз России)
3. Давлианидзе Т.А., Еремина О.Ю. Современные группы инсектицидов: диамиды и мета-диамиды. Весник защиты растений,2021,104 (3), с 132-143
4. Патент номер 1754708 Способ получения фталамида. Авторы: Багирзаде, Гусейнов, Магеррамова, Миратаев, Ризаев, Сулейманов, Шейнин. Институт неорганической и физической химии АН АзССР, 15.08.92 Бил. № 30
5. Хёрд Ч.Д. Пиролиз соединений углерода М.,Л.: Главная редакция химической литературы, 1938 г. – 781 с.
6. Ming Liu , Yi Wang, Wei-zi Wangyang, Feng Liu, Yong-liang Cui, You-sheng Duan, Min Wang, Shang-zhong Liu, Chang-hui Rui. Design, synthesis, and insecticidal activities of phthalamides containing a hydrazone substructure. J Agric Food Chem 2010 Jun 9;58(11):6858-63. doi: 10.1021/jf1000919
7. Patil S.K., Pisal R.H., Deokar H.P. Synthetic method and characterization of novel phthalamide derivatives January 2014 Der Pharma Chemica 6(6):273-278
9. Irac-online.org.
10. PubChem