Химические классы пестицидов
Оглавление
Группы производных тетразина
Тетразины, как и пиридины, диазины, триазины – это полиазины. Так называют углеродистые соединения, по строению структурной формулы напоминающие бензол (имеющие в структуре шестичленное замкнутое кольцо, состоящее из шести атомов), но в отличии от него содержащие вместо углерода от одного до четырех атомов азота[5].
По количеству последних различают: монодиазины (пиридины) – один атом азота; диазины – два азота; триазины – три атома азота и тетразины – четыре[5]. Введение в шестиатомное углеродное кольцо более четырех атомов азота на сегодняшний день невозможно, поскольку с уменьшением углеродных атомов в шестиатомном кольце его прочность снижается, и оно становиться непостоянным и стремиться перейти в более простое пятиатомное кольцо триазола[5].
Тетразин, как первое соединение гомологического ряда тетразины, может быть представлен в форме трех структур с вициальным, симметричным и асимметричным расположением атомов азота. Это 1,2,3,4-тетразин (виц-тетразин), 1,2,4,5-тетразин (симм-тетразин, s-тетразин), 1,2,3,5-тетразин (асимм-тетразин)[5].
Виц-тетразины
Производные 1,2,3,4 – тетразины называют виц-тетразинами. Их делят на три группы:
- соединения с арильными заместителями в положении 2 и 3;
- соединения с бензольными группами в положениях 2 и 3;
- бензо-виц-тетразины[5].
Представителей первых двух групп первоначально именовали 2,3-дигидро-виц-тетразинами или озоттразинами. Они были получены окислением озазонов αβ-дикетонов[5].
Симм-тетразины
Производные 1,2,4,5-тетразина называют симм-тетразинами. Их делят на следующие группы:
- алкильные производные;
- фторалкильные производные;
- арильные производные;
- симм-треазины с гетероциклическими заместителями в положении 3 и 6: производные пиридина, производные пиримидина, производные фурана, производные тиазола, производные пиразола, производные тетразола;
- симм-тетразины с функциональными заместителями: производные карбоновых кислот, аминопроизводные, карбонильные производные, тиокарбонильные производные;
- 1,4-дигидро-симм-тетразины;
- тетра-гидро-симм-тетразины;
- гегса-гидро-симм-тетразины;
- конденсированные симм-тетразиновые системы;
- симм-тетразины с трансаннулярными мостиками;
- симм-тетразиновые кольца, конденсированные с углеводородными циклами;
- симм-тетразиновые кольца, конденсированные с гетероциклами[5].
Действие на вредные организмы
Тетразины могут обладать различной биологической активностью. Есть сведения, что отдельные симм-треазины с гетероциклическими заместителями в положении 3 и 6, могут быть использованы, как действующие вещества системных гербицидов[5].
Тетразины с акарицидной активностью используют в сфере защиты растений. В классификацию IRAC включены:
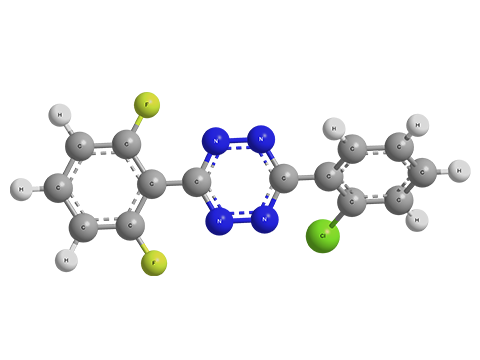
- клофентезин (clofentezine), C14H8Cl2N4, CAS 74115-24-5;
- дифловидазин (diflovidazin) C14H7ClF2N4, CAS 162320-67-4[6][7].
Механизм действия
. По классификации IRAC клофентезин (сlofentezine) и дифловидазин (diflovidazin) отнесены к группе 10 с механизмом действия – ингибиторы роста клещей, влияющие на CHS1/mite growth inhibitors affecting CHS1. Другими словами, механизм действия соединений, отнесенных к группе 10, проявляется в подавлении фермента, катализирующего полимеризацию хитина[6].Кроме клофентезина и дифловидазина этот же механизм действия обнаруживают соединения:
- гекситиазокс, принадлежащее к классу тиазолидины;
- этоксазол (C21H23F2NO2, CAS 153233-91-1), относящееся к классу оксазолины (производные оксазолина, пятичленного гетероцикла с одним атомом азота и одним атомом кислорода)[6][7].
Подробнее о действующих веществах дифловидазин и клофентезин – в статьях «Дифловидазин», «Клофентезин».
Химические классы и соединения, по механизму инсектицидного действия – ингибиторы роста клещей, влияющие на CHS1 (Группа 10 по классификации IRAC):
А. Действующие вещества:
- клофентезин (сlofentezine) – тетразины;
- дифловидазин (diflovidazin) – тетразины;
- гекситиазокс (hexythiazox) – тиазолидины[6].
B. Действующие вещества:
- этоксазол (etoxazole) – оксазолины[6].
Резистентность
– одно из отрицательных последствий применения химических методов борьбы с вредителями растений. Она носит преадаптивный характер и является результатом отбора летальными практически для всей популяции дозами пестицидов[3].Образование популяции, резистентной к пестициду – это микроэволюционный процесс, в течение которого под влиянием химических обработок происходит элиминация «нормальных» особей и выживание мутантов – особей, обладающих физиолого-биохимическим механизмом, толерантным к действию инсектицида или способным к его детоксикации. Мутации устойчивости возникают в природных популяциях спонтанно (вне зависимости от химических обработок) с частотой 10-5–10-6[3].
По мере увеличения доли устойчивых мутантов и частоты скрещиваний между ними происходит скачкообразное возрастание устойчивости, элиминация чувствительных и толерантных особей и стабилизация резистентности на предельно высоком для конкретного препарата уровне[3].
Мутация устойчивости может оказать и плейотропное действие на биологические показатели резистентных особей, но в период отбора (обработки акарицидами) приспособительная ценность селектируемого генотипа практически не имеет значения, так как основное – обладание фактором (геном) устойчивости[3].
Сохранение резистентности после прекращения обработок зависит от биотического потенциала и конкурентной способности особей с нормальным и резистентным генотипами[3].
Наблюдения за потерей резистентности позволило выявить три тира реверсии:
- стабильная резистентность – сохраняется после прекращения обработок неопределенно долгое время (более 100 поколений вредителя), селектируется динитропроизводными, производными сульфокислот, овицидами, ингибиторами синтеза хитина;
- нестабильная резистентность с медленным уменьшением уровня после прекращения обработок (в течение 20–30 генераций), селектируется хлорорганическими акарицидами;
- нестабильную резистентность с быстрым уменьшением уровня после прекращения обработок данным препаратом, селектируется фосфорорганическими акарицидами, устойчивость к которым клещи теряют спустя 10–12 генераций после прекращения обработок[3].
В случае возникновения резистентности следует немедленно принять меры к разработке и выполнению мероприятий по ее преодолению с учетом реверсии и механизма приобретенной устойчивости. Отмечается, что при нестабильной резистентности с быстрым снижением уровня устойчивости, вновь применять соединения, сформировавшие резистентность возможно только через 1–2 года, но не более одного раза за сезон. При стабильной резистентности применение селектирующего резистентность препарата даже через 3–5 лет приводит к ее восстановлению[2].
Знание механизма приобретения резистентности позволяет быстро найти нетрадиционные приемы ее преодоления, но в любом случае выгоднее не допускать развития резистентности, чем искать приемы ее преодоления[2].
Профилактика резистентности
. Борьба с резистентными популяциями усложнена тем, что любое мероприятие, направленное на уничтожение чувствительных особей (повышение эффективности препарата, совершенствование способа обработки и прочее) идет на пользу устойчивым особям. Чем выше эффективность применения препарата, тем быстрее развивается резистентность и тем быстрее он становится нетоксичным для обрабатываемой популяции. Неправильная замена на другое действующее вещество или применение смеси действующих веществ может привести к развитию перекрестной или множественной резистентности[2].Путем анализа закономерностей развития резистентности была выработана система защиты, в основу которой положены генетические принципы. Для предупреждения резистентности рекомендуется не произвольная замена одного действующего вещества на другое, а чередование соединений из групп с различным механизмом действия таким образом, чтобы при скрещивании особей с различным типом устойчивости в потомстве не выщеплялись формы с множественной устойчивостью[2].
Такая замена обеспечивается и при использовании действующих веществ согласно распределению по группам классификации IRAC[6].
Установлено, что чередование трех правильно подобранных препаратов предотвращает повышение устойчивости популяции вредителя на протяжении 300 поколений, что позволяет не снижать эффективность обработок в течение многих лет[2].
В сфере защиты растений от вредителей, в том числе клещей, важны мероприятия, позволяющие замедлить процесс отбора. К ним относятся:
- неукоснительное соблюдение рекомендуемых норм расхода препарата;
- сохранение энтомофагов;
- чередование химических и нехимических мер борьбы[2].
Применение
Тетразины используют в различных отраслях химической промышленности. Производные симм-тразина используют для получения полимеров, красителей, антиоксидантов и стабилизаторов для природных и синтетических углеводородных полимеров, и ненасыщенных масел. Тетразины, полученные окислением используются как десенсибилизаторы в фотографии[5].
Тетразины, используемые в сфере защиты растений относятся к группе симм-треазинов с гетероциклическими заместителями в положении 3 и 6[5].
В настоящее время для использования в сфере защиты растений в качестве действующих веществ акарицидов применяют следующие тетразины: клофентезин и дифловидазин[6].
В «Государственный каталог пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации, 2024 год.» внесены акарициды с действующим веществом дифловидазин и клофентезин[1].
Токсикологические свойства и характеристики
Тетразины, используемые в сфере защиты растений, относятся к умерено токсичным веществам в отношении человека и млекопитающих и малотоксичным в отношении пчел. Использование препаратов, содержащих тетразины, при соблюдении регламента применения, хранения и транспортировки не представляет опасности для окружающей среды[1].
Подробнее о токсикологических свойствах и характеристиках дифловидазина и клофентезина – в статьях «Дифловидазин», «Клофентезин».
История
1,2,4,5-тетразин (симм-тетразин) впервые был синтезирован в 1900 г Генчем и Лема путем декарбоксилированием симм-тетразиндикарбоновой-3,6 кислоты[5].
2. Зинченко В.А. Химическая защита растений: средства, технология и экологическая безопасность. – М.: «КолосС», 2012. – 127 с.
3. Лившиц И.З., Митрофанов В.И., Петрушов А.З. Сельскохозяйственная акарология. М.: 2009 – 345 с.
4. Попов С.Я.; Бурбенцов С.А. Обнаружение фумигационного действия акарицида флумайта (флуфензина) на яйца паутинного клеща [Опыты на Tetranychus atlanticus]. Докл. ТСХА / Московская с.-х. акад. им. Тимирязева. Москва, 2005; Вып. 277. - С. 183-185
5. Эльдерфильд Р. Гетероциклические соединения том 8. Перевод с английского Яшунского В.Г. Издательство «Мир», Москва,1969 – 365 стр.
7. PubChem